
HEMLIBRA 150 mg/ml oldatos injekció
HEMLIBRA 150 mg/ml oldatos injekció betegtájékoztatója
1. Milyen típusú gyógyszer a Hemlibra és milyen betegségek esetén alkalmazható?
Milyen típusú gyógyszer a Hemlibra?
A Hemlibra hatóanyaga az "emicizumab". Ez a gyógyszerek "monoklonális ellenanyagok" elnevezésű csoportjába tartozik. A monoklonális ellenanyagok olyan típusú fehérjék, amelyek felismernek egy bizonyos célpontot a szervezetben és kötődnek ahhoz.
Milyen betegségek esetén alkalmazható a Hemlibra?
A Hemlibra olyan gyógyszer, amely bármely életkorban alkalmazható hemofília A-ban (veleszületett VIII-as faktor hiány) szenvedő betegek kezelésére, akiknél:
- VIII-as faktor elleni gátlóanyagok alakultak ki
- nem alakultak ki VIII-as faktor elleni gátlóanyagok és:
-- súlyos betegségben (a VIII-as faktor szintje a vérben kevesebb mint 1%) szenvednek
-- közepesen súlyos betegségben (a VIII-as faktor szintje a vérben 1% és 5% közötti) szenvednek, súlyos vérzéses fenotípussal.
A hemofília A egy veleszületett rendellenesség, melyet a véralvadáshoz és bármilyen vérzés megállításához nélkülözhetetlen VIII-as faktor hiánya okoz.
Ez a gyógyszer megelőzi a vérzéseket vagy csökkenti a vérzéses epizódok számát az említett betegséggel élőknél.
A hemofília A-ban szenvedő betegek némelyikénél VIII-as faktor elleni gátlóanyagok képződhetnek (VIII-as faktor elleni antitestek), amelyek megakadályozzák, hogy a pótlásként alkalmazott VIII-as faktor kifejtse a hatását.
Hogyan fejti ki a hatását a Hemlibra?
A Hemlibra helyreállítja a hatékony véralvadáshoz szükséges aktivált VIII-as faktor hiányzó funkcióját. A Hemlibra szerkezete eltérő a VIII-as faktor szerkezetétől, így a VIII-as faktor elleni gátló anyagok nem befolyásolják a Hemlibra hatását.
2. Tudnivalók a Hemlibra alkalmazása előtt
Ne alkalmazza a Hemlibra-t
- ha allergiás az emicizumabra vagy a gyógyszer (6. pontban felsorolt) bármely egyéb összetevőjére. Ha nem biztos ebben, a Hemlibra alkalmazása előtt kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert
Figyelmeztetések és óvintézkedések
Nagyon fontos, hogy a Hemlibra alkalmazásának megkezdése előtt beszéljen kezelőorvosával a megkerülő aktivitású hatóanyagot tartalmazó (bypassing) (a véralvadást elősegítő gyógyszerek, melyek a VIII-as faktortól eltérő módon működnek) készítmények alkalmazásáról. Ez azért fontos, mert a megkerülő aktivitású (bypassing) készítményekkel történő kezelés változására szükség lehet a Hemlibra-terápia idején. Megkerülő aktivitású (bypassing) hatóanyag például az "aktivált protrombinkomplex-koncentrátum" (aPCC) és az "aktivált rekombináns VII-es faktor" (rFVIIa).
Súlyos és akár életveszélyes mellékhatások fordulhatnak elő, amikor az aPCC-t olyan betegeknél alkalmazzák, akik egyidejűleg Hemlibra-t is kaptak.
Potenciálisan súlyos mellékhatások a Hemlibra-kezeléssel egyidejű aPCC alkalmazás esetén:
- Vörösvértest pusztulás (trombotikus mikroangiopátia)
-- Ez egy súlyos és potenciálisan életveszélyes állapot.
-- A betegeknél ebben az állapotban az erek falának belső felszíne károsodhat, és a kis erekben vérrögök keletkezhetnek. Néhány esetben ez a vese és/vagy más szervek károsodását okozhatja.
-- Legyen óvatos, ha Önnél magas ennek az állapotnak a kockázata (korábban már előfordult Önnél ez az állapot vagy valamely családtagja szenvedett ettől), vagy ha olyan gyógyszereket szed, melyek növelhetik ezen állapot kifejlődésének a kockázatát, ilyen például a ciklosporin, kinin vagy takrolimusz.
-- Fontos, hogy felismerje a trombotikus mikroangiopátia tüneteit, ha esetleg ilyen állapot kialakulna Önnél (a tünetek felsorolása a 4. pontban található, "Lehetséges mellékhatások").
Hagyja abba a Hemlibra és az aPCC alkalmazását, és azonnal forduljon orvoshoz, ha Ön vagy gondozója a trombotikus mikroangiopátia bármilyen tünetét észleli.
- Vérrögök (tromboembólia)
-- Ritka esetekben vérrög keletkezhet az erekben és elzárhatja az ereket, mely életveszélyes lehet.
-- Fontos, hogy felismerje az ilyen vérrögképződés tüneteit, ha esetleg vérrög alakulna ki Önnél (a tünetek felsorolása a 4. pontban található, "Lehetséges mellékhatások").
Hagyja abba a Hemlibra és az aPCC alkalmazását, és azonnal forduljon orvoshoz, ha Ön vagy gondozója az erekben történő vérrögképződés bármilyen tünetét észleli.
Egyéb fontos információk a Hemlibrával kapcsolatban
- Antitestképződés (immunogenitás)
-- Azt tapasztalhatja, hogy a vérzés nem kontrollálható a gyógyszer előírt adagjával. Ez azért lehet, mert ellenanyag képződik ezzel a gyógyszerrel szemben.
Azonnal keresse fel kezelőorvosát, ha Ön vagy gondozója azt észleli, hogy a vérzések fokozódnak. Előfordulhat, hogy kezelőorvosa úgy dönt, megváltoztatja a kezelést, ha ez a gyógyszer már nem hat Önnél.
1 évesnél fiatalabb gyermekek
Az egy éves kor alatti gyermekeknél a vérkeringési rendszer még mindig fejlődik. Amennyiben az Ön gyermeke egy évesnél fiatalabb, a kezelőorvosa kizárólag a készítmény alkalmazásához köthető előnyök és kockázatok gondos mérlegelése után írhat fel Hemlibra-t az Ön gyermeke számára.
Egyéb gyógyszerek és a Hemlibra
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben alkalmazott, valamint alkalmazni tervezett egyéb gyógyszereiről.
- Megkerülő aktivitású (bypassing) hatóanyagot tartalmazó készítmény alkalmazása a Hemlibra-kezelés ideje alatt
-- A Hemlibra alkalmazásának megkezdése előtt beszéljen kezelőorvosával, és gondosan kövesse az útmutatásait arra vonatkozóan, hogy megkerülő aktivitású hatóanyagot tartalmazó készítményt, mikor, milyen adagban és milyen ütemezés szerint alkalmazzon. A Hemlibra fokozza a vér alvadási készségét. Ezért a megkerülő aktivitású hatóanyagot tartalmazó készítményből kisebb adagra lehet szükség, mint amelyet a Hemlibra alkalmazása előtt kapott.
-- Csak akkor alkalmazza az aPCC-t, ha más kezelési lehetőség nem áll rendelkezésre. Ha azonban aPCC alkalmazása szükséges, beszéljen kezelőorvosával, ha úgy érzi, hogy összesen 50 egység/ttkg adagnál több aPCC beadását igényli. Az aPCC Hemlibra-kezelés ideje alatti alkalmazásáról a 2. pontban talál bővebb információt: "Potenciálisan súlyos mellékhatások a Hemlibra-kezeléssel egyidejű aPCC alkalmazás esetén".
-- Annak ellenére, hogy korlátozott tapasztalat áll rendelkezésre az anti-fibrinolitikumok aPCC-vel vagy aktivált rekombináns VII-es faktorral való együttes alkalmazásáról Hemlibra-val kezelt betegeknél, tudnia kell, hogy fennállhat a trombózisos események lehetősége anti-fibrinolitikumok intravénás alkalmazásakor aPCC-vel vagy aktivált rekombináns VII-es faktorral való kombináció esetén.
Laboratóriumi vizsgálatok
A véralvadás jellemzőit mérő laboratóriumi vizsgálatok előtt mondja el kezelőorvosának, hogy Hemlibra-t alkalmaz. Erre azért van szükség, mert a Hemlibra jelenléte a vérben befolyásolhatja a laboratóriumi vizsgálatok egy részét, ami pontatlan eredményekhez vezet.
Terhesség és szoptatás
- A Hemlibra-kezelés ideje alatt és a Hemlibra utolsó injekciójának beadását követő 6 hónapban hatékony fogamzásgátló módszert kell alkalmaznia.
- Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével. Kezelőorvosa mérlegelni fogja a Hemlibra-kezelés Önnél várható előnyeit a gyermekét érintő kockázattal szemben.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Nem valószínű, hogy ez a gyógyszer befolyásolja a gépjárművezetéshez és a gépek kezeléséhez szükséges képességeket.
3. Hogyan kell alkalmazni a Hemlibra-t?
A Hemlibra egyszer használatos injekciós üvegekben található, mint beadásra kész oldat, hígítani nem szükséges. A Hemlibra-kezelést egy vérzékeny betegek ellátásában jártas orvos fogja elindítani. A gyógyszert mindig a kezelőorvosa által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát.
Napló vezetése
A Hemlibra minden egyes alkalmazásakor írja fel a gyógyszer nevét és gyártási tételének számát.
Mennyi Hemlibra-t kell alkalmazni?
A Hemlibra adagja az Ön testtömegétől függ, és kezelőorvosa ki fogja számítani a Hemlibra beadandó szükséges mennyiségét (mg-ban) és a neki megfelelő oldat térfogatát (ml-ben).
- Telítő dózis: 1-4. hét: Az adag testtömegkilogrammonként 3 milligramm, hetente egyszer, injekcióként beadva.
- Fenntartó dózis: Az 5. héttől kezdve: Az adag vagy testtömegkilogrammonként 1,5 milligramm, hetente egyszer, injekcióként beadva, vagy testtömegkilogrammonként 3 milligramm, kéthetente, injekciónként alkalmazva vagy testtömegkilogrammonként 6 milligramm, négyhetente, injekciónként alkalmazva.
A hetente egyszer 1,5 mg/ttkg, kéthetente 3 mg/ttkg, vagy négyhetente 6 mg/ttkg fenntartó dózist alkalmazásáról való döntést a kezelőorvossal és ha releváns a gondozóval kell megbeszélni.
Az alkalmazandó teljes térfogat elkészítésénél a különböző koncentrációjú Hemlibra készítmények (30 mg/ml és 150 mg/ml) nem kombinálhatóak egyetlen injekcióban.
A beadandó Hemlibra oldat mennyisége injekciónként 2 ml-nél nagyobb nem lehet.
Hogyan kell a Hemlibra-t beadni?
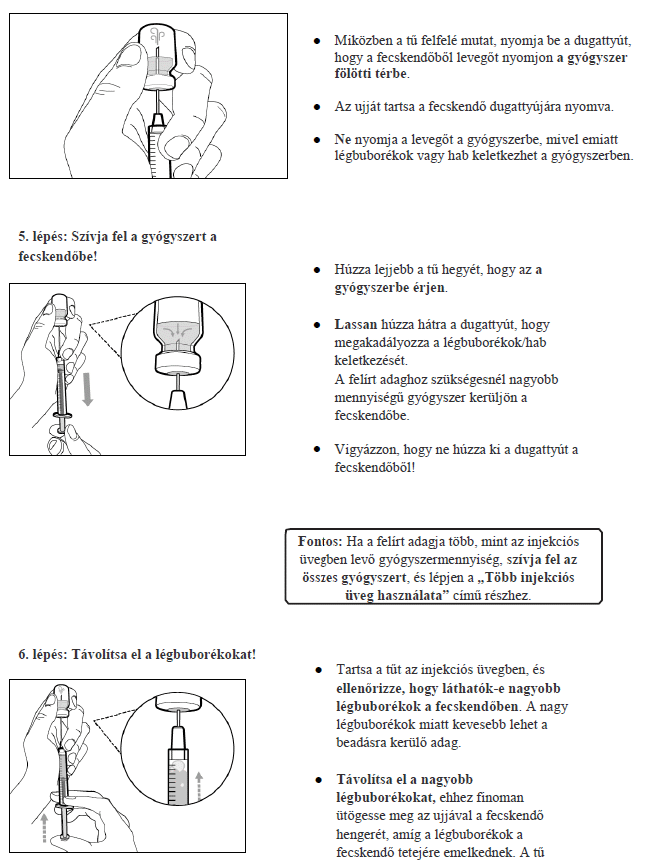
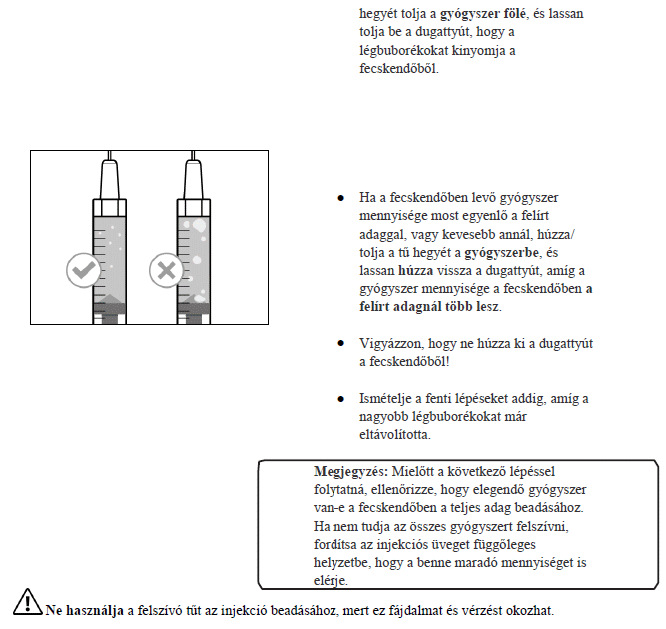
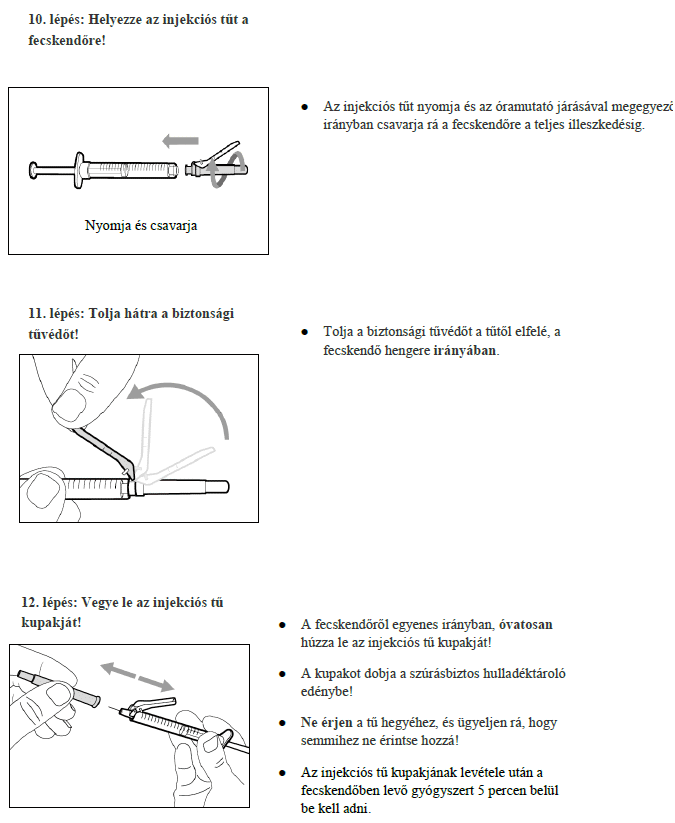
Ha Ön vagy gondozója adja be a Hemlibra injekciót, gondosan el kell olvasnia és követnie kell Önnek vagy gondozójának a "Használati utasítás" című 7. pontban szereplő útmutatást.
- A Hemlibra-t bőr alá adott (szubkután) injekcióval kell alkalmazni.
- Kezelőorvosa vagy a gondozását végző egészségügyi szakember megmutatja Önnek, hogyan kell a Hemlibra injekciót beadni.
- Ha Ön oktatásban részesült, otthon, önállóan vagy a gondozó segítségével be kell tudnia adni a gyógyszert.
- Ahhoz, hogy a tűt megfelelően szúrja a bőr alá, a szabad kezével fogjon össze lazán egy bőrredőt az injekció beadásának megtisztított helyén. A bőrredő összefogása fontos annak érdekében, hogy a készítményt bőr alá (zsírszövetbe), de ne mélyebbre (izomba) fecskendezze. Az izomba adott injekció kellemetlen lehet.
- Az injekció előkészítését és beadását tiszta és csíramentes körülmények között, "aszeptikus technika" alkalmazásával végezze. Erről a kezelőorvos vagy a gondozását végző egészségügyi szakember fogja részletesebben tájékoztatni.
Hová adja a Hemlibra injekciót?
- Kezelőorvosa megmutatja Önnek, hogy a Hemlibra injekciót a test mely területeire kell beadni.
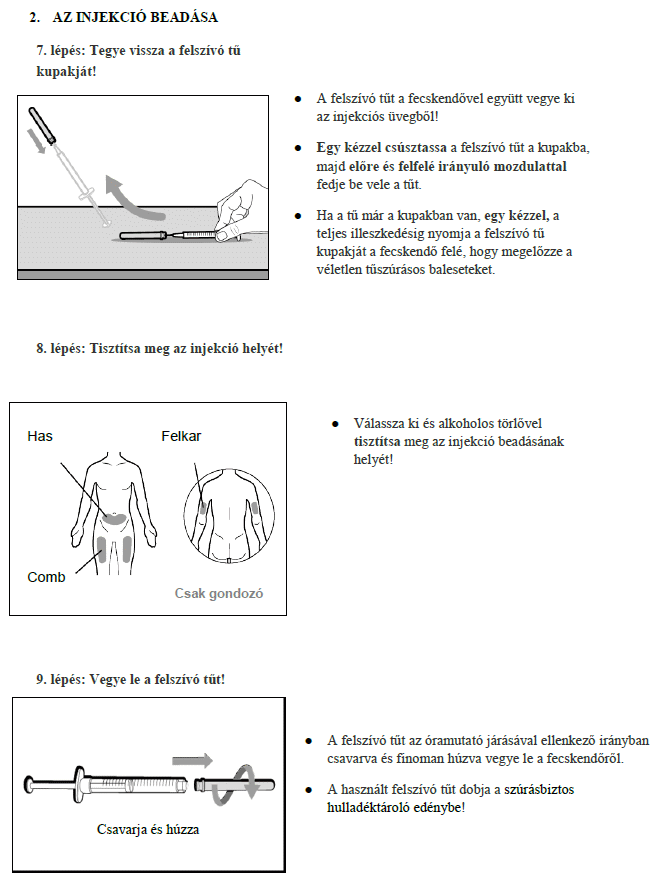
- Az injekció beadására javasolt helyek: a has alsó része, a felkar külső felszíne, valamint a comb elülső része. Kizárólag a javasolt helyekre adjon be injekciót!
- Minden alkalommal az előzőtől eltérő testtájra kell beszúrni az injekciót.
- Az injekciókat ne adja olyan helyre, ahol a bőrön bőrpír, véraláfutás, érzékenység vagy kemény terület észlelhető, illetve anyajegyek vagy hegek területére.
- A Hemlibra alkalmazásakor az egyéb, bőr alá fecskendezett gyógyszereket más területre kell beadni.
Fecskendők és tűk használata
- Egy fecskendőt, egy 5 mikrométeres szűrővel ellátott felszívó tűt vagy egy 5 mikrométeres szűrővel ellátott injekciósüveg-adaptert és egy injekciós tűt használnak ahhoz, hogy a Hemlibra oldatot az injekciós üvegből felszívják a fecskendőbe, és a bőr alá beadják.
- A fecskendők, szűrővel ellátott felszívó tűk vagy a szűrővel ellátott injekciósüveg-adapter és injekciós tűk nem találhatók meg ebben a csomagolásban. Bővebb információa 6. pontban található "Mi szükséges még a Hemlibra beadásához ami nem található ebben a csomagolásban?" cím alatt.
- Ügyeljen rá, hogy minden injekcióhoz új injekciós tűt használjon, és egyszeri használat után dobja ki.
- Legfeljebb 1 ml-es Hemlibra oldat injekcióként történő beadásához 1 ml-es fecskendőt kell használni.
- 1 ml-nél nagyobb és legfeljebb 2 ml-es Hemlibra oldat injekcióként történő beadásához 2-3 ml-es fecskendőt kell használni.
Alkalmazás gyermekeknél és serdülőknél
A Hemlibra bármilyen korú gyermekeknél és serdülőknél alkalmazható.
- Egy gyermek beadhatja saját magának a gyógyszert, a gyermek gondozását végző egészségügyi szakember és a szülő vagy gondozó beleegyezése esetén. Az öninjekciózás 7 évesnél fiatalabb gyermekek esetében nem ajánlott.
Ha az előírtnál több Hemlibra-t alkalmazott
Ha Ön az előírtnál több Hemlibra-t alkalmazott, azonnal tájékoztassa a kezelőorvosát. Ez azért szükséges, mert fennállhat a mellékhatások, például vérrögök kialakulásának kockázata. A Hemlibra-t mindig pontosan a kezelőorvosa által elmondottaknak megfelelően alkalmazza, és bizonytalanság esetén kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
Ha elfelejtette alkalmazni a Hemlibra-t
- Ha elfelejti a tervezett injekciót, adja be az elfelejtett adagot, amint lehet, a következő tervezett adag napja előtt. Ezután a tervezett módon folytassa a gyógyszer egyszer esedékes injekcióit. Ne adjon be egy napon két adagot a kihagyott adag pótlására.
- Ha nem biztos abban, hogy mit kell tennie, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
Ha abbahagyja a Hemlibra alkalmazását
Ne hagyja abba a Hemlibra alkalmazását anélkül, hogy ezt kezelőorvosával megbeszélné. Ha abbahagyja a Hemlibra alkalmazását, lehetséges, hogy már nem lesz védve a vérzésekkel szemben.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Az aPCC alkalmazásának súlyos mellékhatásai Hemlibra-kezelés ideje alatt
Hagyja abba a Hemlibra és az aPCC alkalmazását, és azonnal beszéljen egy orvossal, ha Ön vagy gondozója az alábbi mellékhatások bármelyikét észleli:
- Vörösvértest pusztulás (trombotikus mikroangiopátia):
-- zavartság, gyengeség, a karok és a lábak feldagadása, a bőr és a szemek besárgulása, nem körülírható hasi fájdalom vagy hátfájás, hányinger, hányás vagy csökkent vizeletürítés - ezek a tünetek a trombózisos mikroangiopátia jelei lehetnek.
- Vérrögök (tromboembólia):
-- duzzanat, melegség, fájdalom vagy vörösség - ezek a tünetek a bőr felszínéhez közel eső vénában keletkezett vérrög jelei lehetnek.
-- fejfájás, az arc zsibbadása, a szem fájdalma vagy duzzanata vagy látásromlás - ezek a tünetek a szem mögötti vénában keletkezett vérrög jelei lehetnek.
-- a bőr elfeketedése - ez a tünet a bőrszövet súlyos károsodásának jele lehet.
Egyéb mellékhatások a Hemlibra alkalmazása során
Nagyon gyakori: 10 beteg közül 1-nél többet érinthet
- reakció az injekció beadásának helyén (bőrpír, viszketés, fájdalom)
- fejfájás
- ízületi fájdalom
Gyakori: 10 beteg közül legfeljebb 1-et érinthet
- láz
- izomfájdalom
- hasmenés
- viszkető kiütés vagy csalánkiütés (urtikária)
- bőrkiütés
Nem gyakori: 100 beteg közül legfeljebb 1-et érinthet
- vörösvértest pusztulás (trombotikus mikroangiopátia)
- vérrög a szem mögötti vénában (szinusz kavernozusz trombózis)
- a bőrszövet súlyos károsodása (bőrelhalás)
- vérrög a bőr felszínéhez közel eső vénában (felületes tromboflebitisz)
- arc-, nyelv- és/vagy torokduzzanat és/vagy nyelési nehézség vagy csalánkiütés légzési nehézséggel társulva angioödémára utalhatnak
- a hatás hiánya vagy csökkent válasz a kezelésre
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a https://mellekhatas.ogyei.gov.hu/ weboldalon. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Hemlibra-t tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A dobozon és a címkén feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Hűtőszekrényben (2 °C - 8 °C) tárolandó. Nem fagyasztható!
A fénytől való védelem érdekében tartsa az eredeti csomagolásban.
Ha a hűtőszekrényből kivették, a bontatlan injekciós üvegek legfeljebb 7 napig tarthatók szobahőmérsékleten (30 °C alatt). Szobahőmérsékleten való tárolást követően a bontatlan injekciós üvegek a hűtőszekrénybe visszahelyezhetők. A gyógyszer szobahőmérsékleten való tárolásának összesített időtartama nem haladhatja meg a 7 napot.
Dobja ki azokat az injekciós üvegeket, amelyek több mint 7 napig voltak szobahőmérsékleten vagy amelyeket, 30 °C feletti hőmérsékleten tárolt.
Ha a Hemlibra-t az injekciós üvegből felszívták a fecskendőbe, azonnal fel kell használni. A fecskendőben levő oldatot ne tegye hűtőszekrénybe.
A gyógyszer felhasználása előtt ellenőrizze, hogy láthatók-e az oldatban részecskék vagy elszíneződés. Az oldatnak színtelennek vagy enyhén sárgásnak kell lennie. Ne használja fel a gyógyszert, ha az homályos, elszíneződött vagy látható részecskéket tartalmaz.
A fel nem használt oldatot megfelelően ki kell dobni. Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Hemlibra?
- Hatóanyaga az emicizumab. A Hemlibra injekciós üvegenként 60 mg (0,4 ml 150 mg/ml koncentrációban), 105 mg (0,7 ml 150 mg/ml-es koncentrációban), 150 mg (1 ml 150 mg/ml-es koncentrációban) vagy 300 mg (2 ml 150 mg/ml-es koncentrációban) emicizumabot tartalmaz.
- További összetevői: L-arginin, L-hisztidin, L-aszparaginsav, poloxamer 188 és injekcióhoz való víz.
Milyen a Hemlibra külleme és mit tartalmaz a csomagolás?
A Hemlibra egy oldatos injekció. A Hemlibra színtelen/enyhén sárgás folyadék.
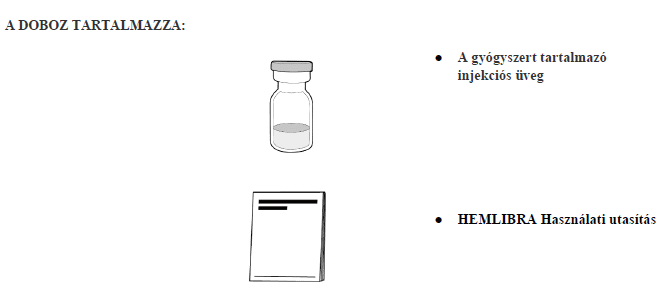
A Hemlibra minden csomagja 1 injekciós üveget tartalmaz.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
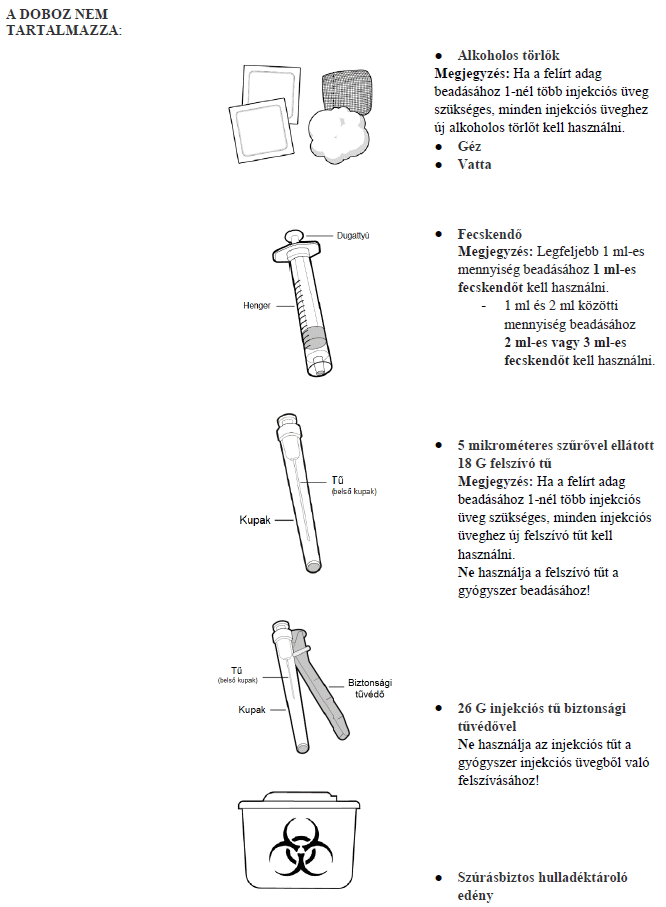
Mi szükséges még a Hemlibra beadásához, ami nem található ebben a csomagban?
Egy fecskendőre, egy szűrővel ellátott felszívótűre vagy szűrővel ellátott injekciósüveg-adapterre és egy injekciós tűre van szükség ahhoz, hogy a Hemlibra oldatot az injekciós üvegből egy fecskendőbe felszívják és a bőr alá fecskendezzék (lásd 7. pont, "Használati utasítás").
Fecskendők
- 1 ml-es fecskendő: Átlátszó polipropilén vagy polikarbonát fecskendő Luer-záras tűvel, 0,01 ml-enkénti osztással, vagy
- 2-3 ml-es fecskendő: Átlátszó polipropilén vagy polikarbonát fecskendő Luer-záras tűvel, 0,1 ml-enkénti osztással.
Megjegyzés: Kis holtterű (LDS) dugattyúval ellátott fecskendőket kell használni a szűrővel ellátott injekciósüveg-adapter használatakor.
Felszívó eszközök és tűk
- Szűrővel ellátott felszívó tű: Rozsdamentes acél, Luer-záras csatlakozós, külső átmérője 18 G, hossza 35 mm (11/2″), 5 mikrométeres szűrővel ellátott, lehetőleg félig tompa heggyel, vagy
- Szűrővel ellátott injekciósüveg-adapter: polipropilén, Luer-záras csatlakozós, 5 mikrométeres szűrővel, 15 mm-es injekciós üveg nyakátmérővel és
- Injekciós tű: Rozsdamentes acél, Luer-záras csatlakozós, külső átmérője 26 G (elfogadható tartomány: 25 - 27 G), hossza lehetőleg 9 mm (3/8″) vagy legfeljebb 13 mm (1/2″), lehetőleg a biztonsági tűvédő elemet is beleértve.
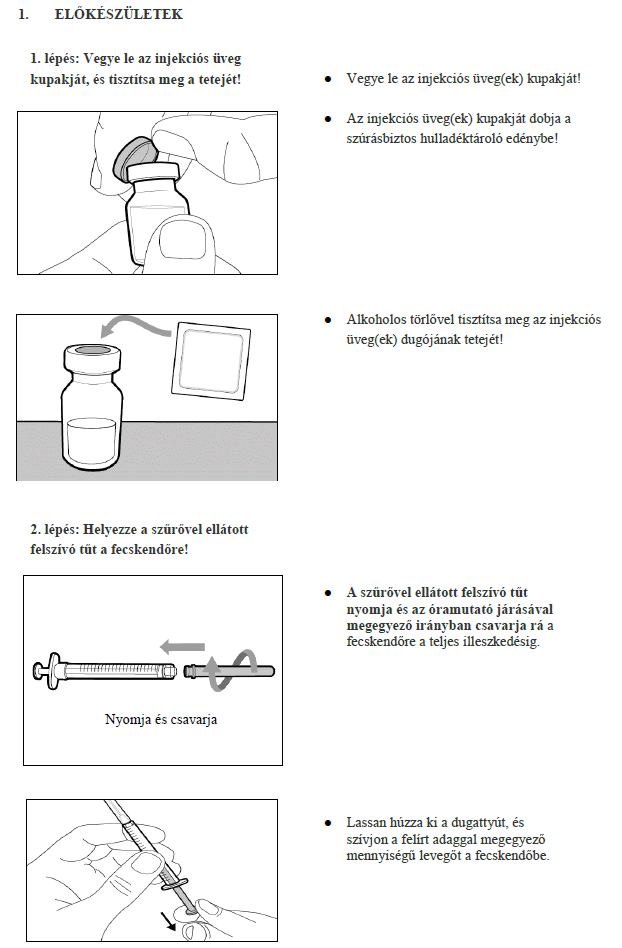
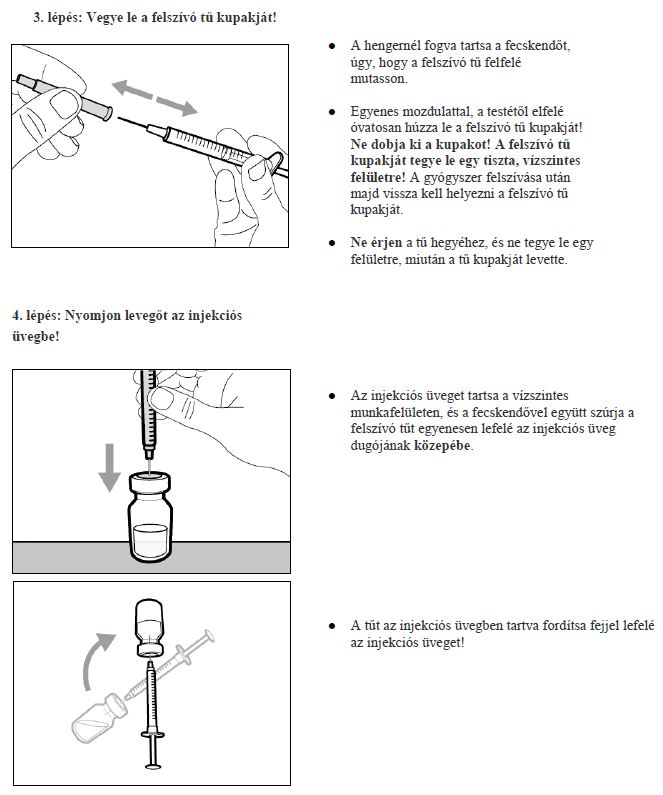
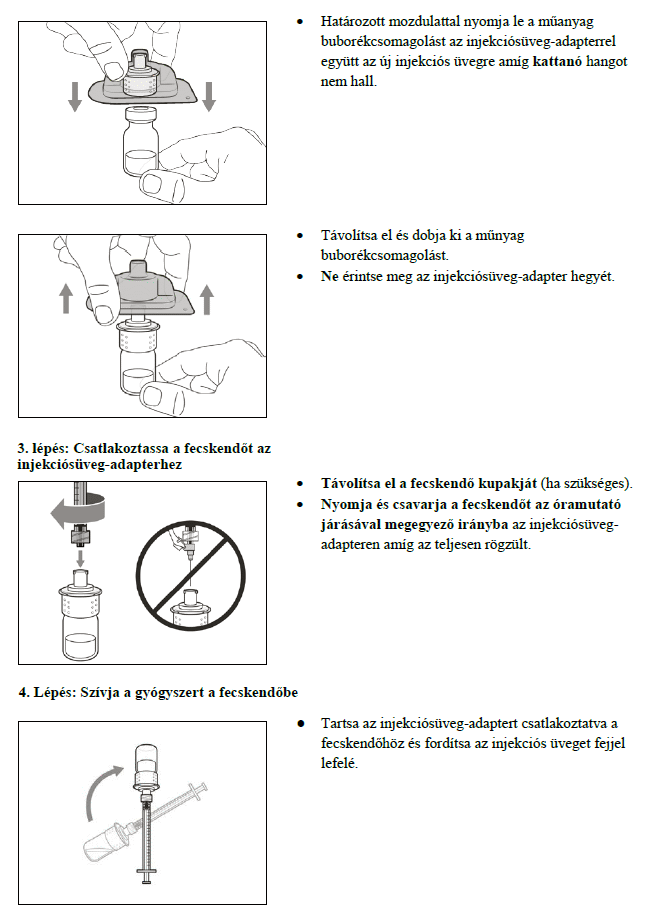
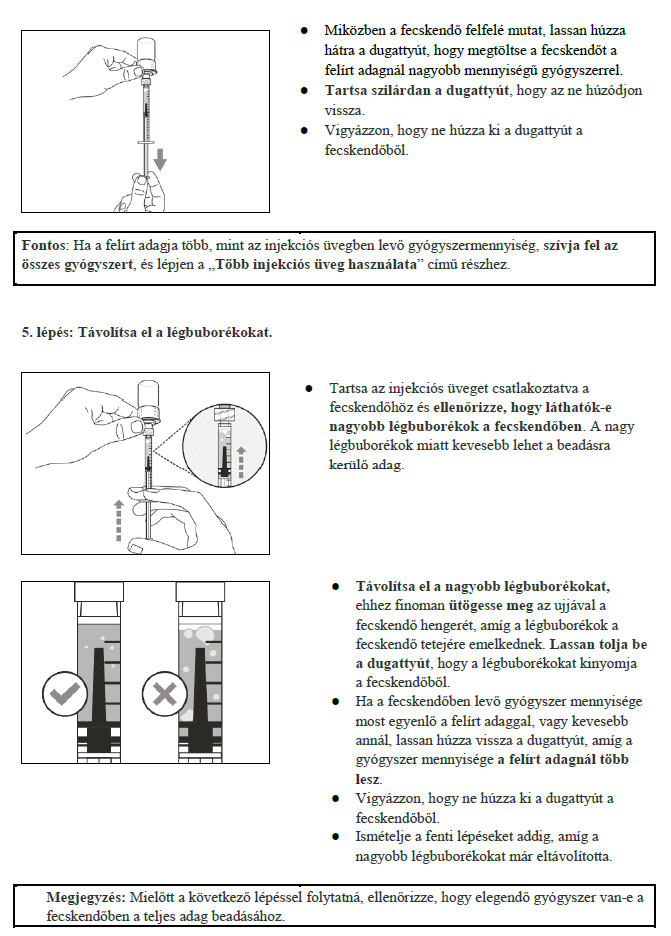
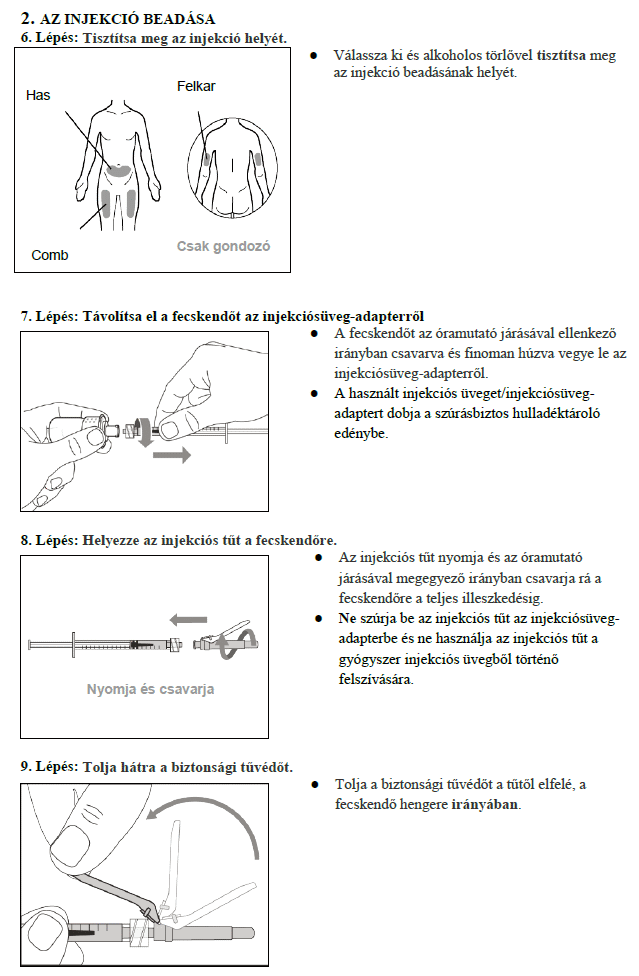
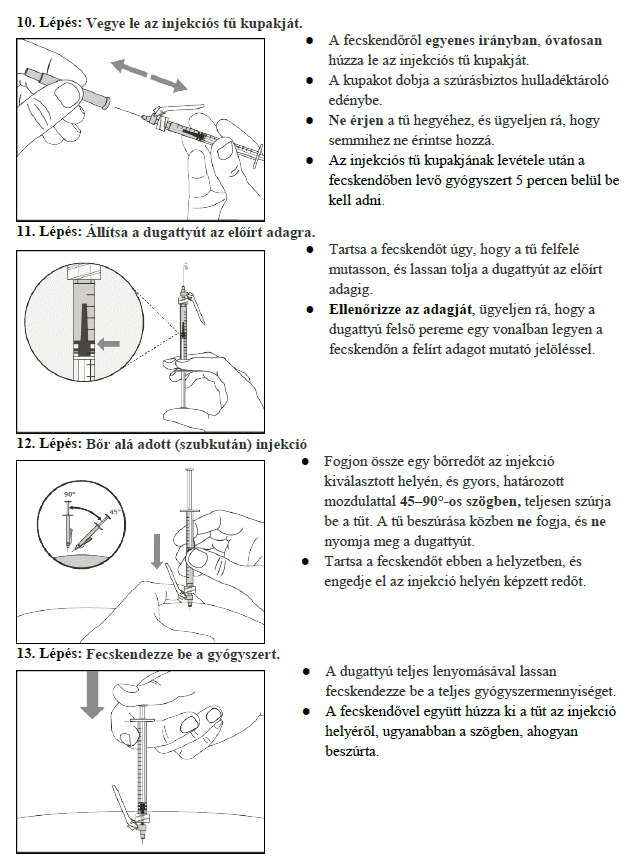
7. Használati utasítás




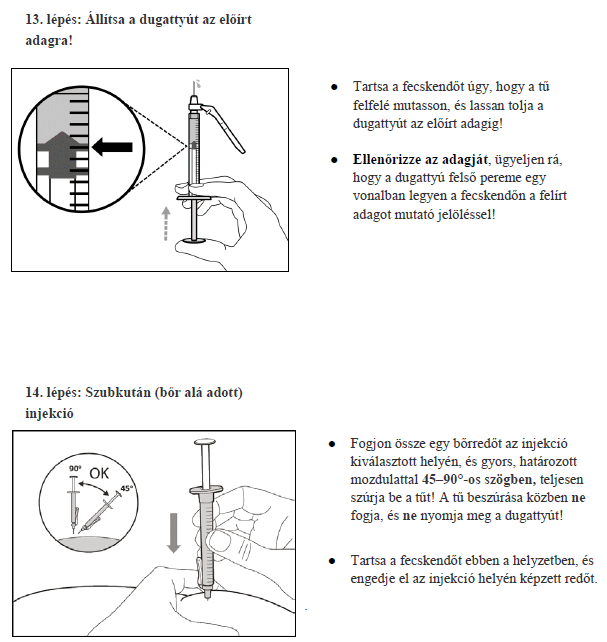
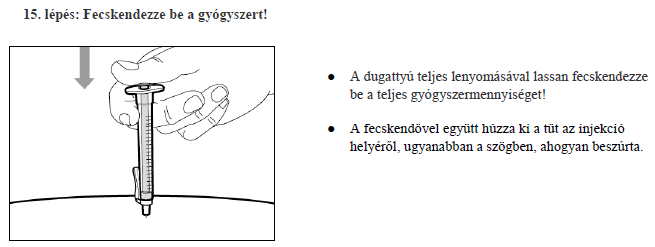
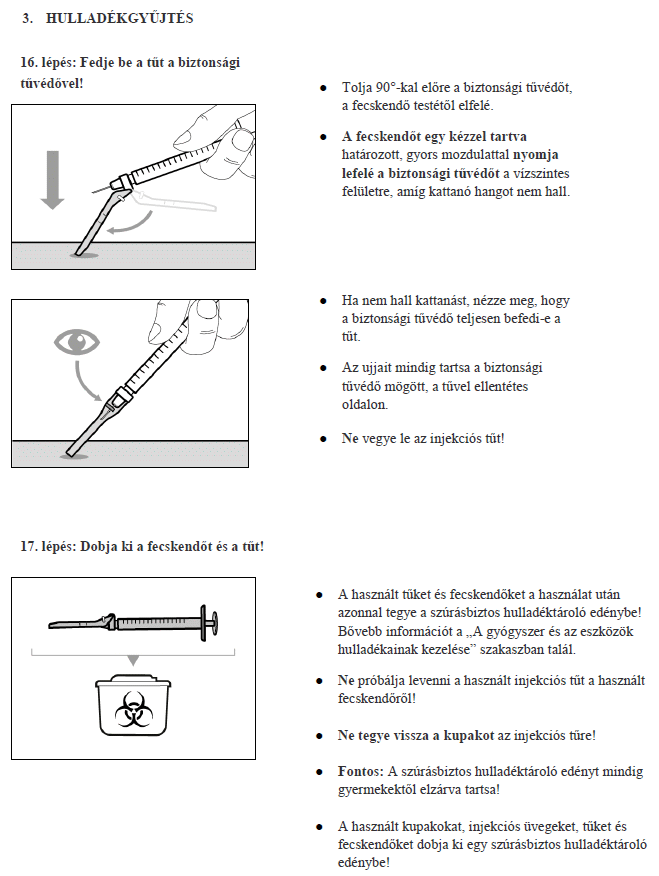
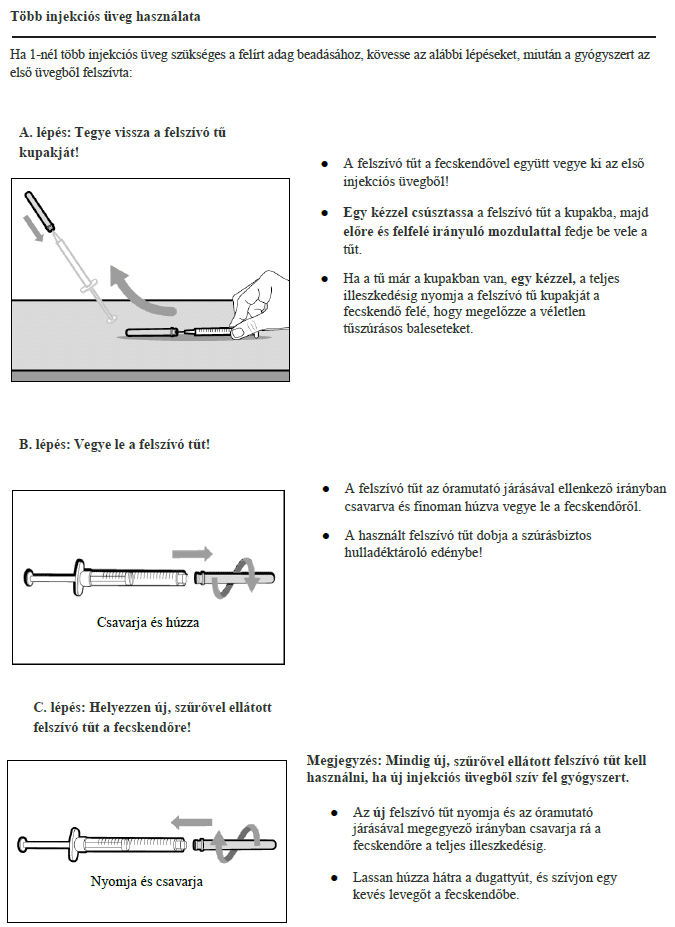
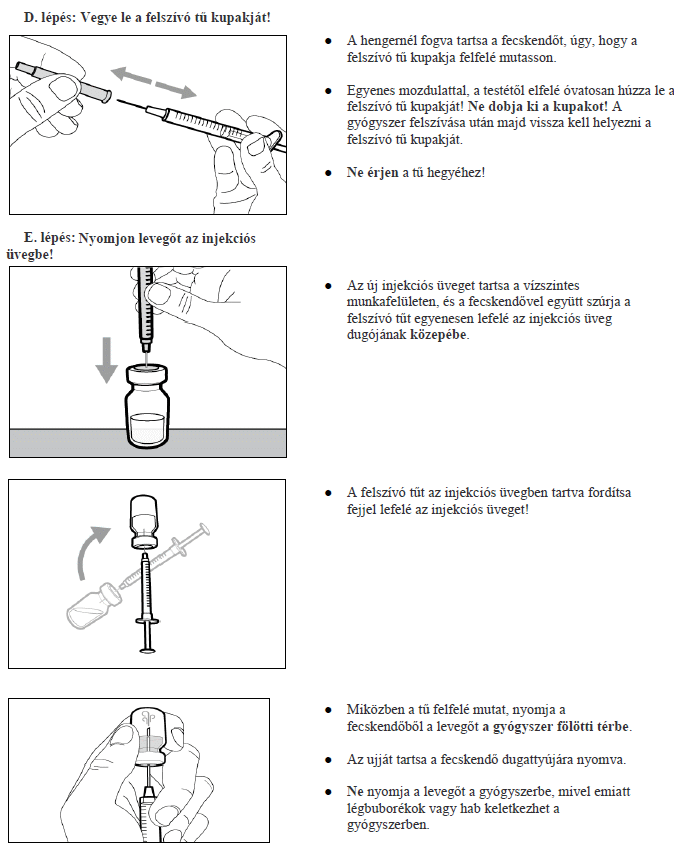
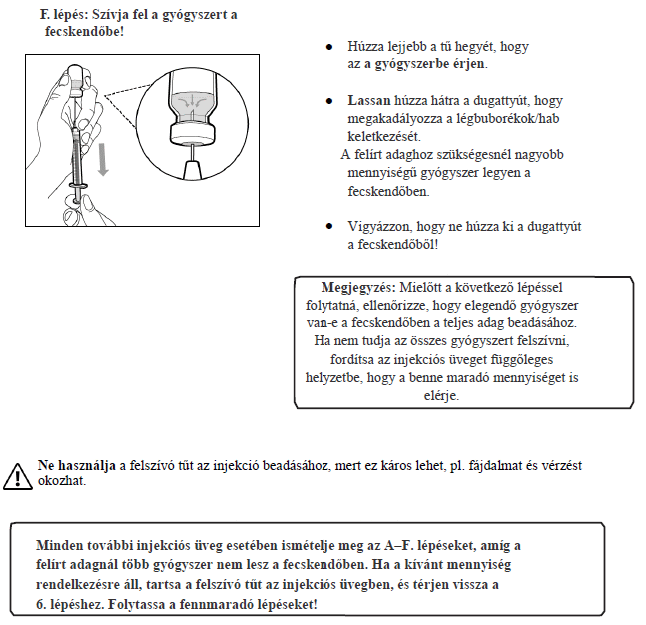


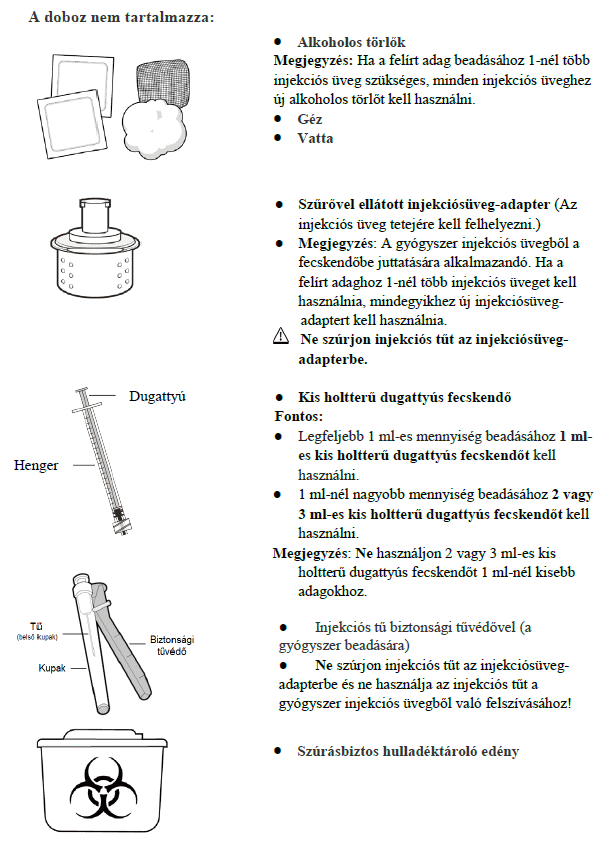


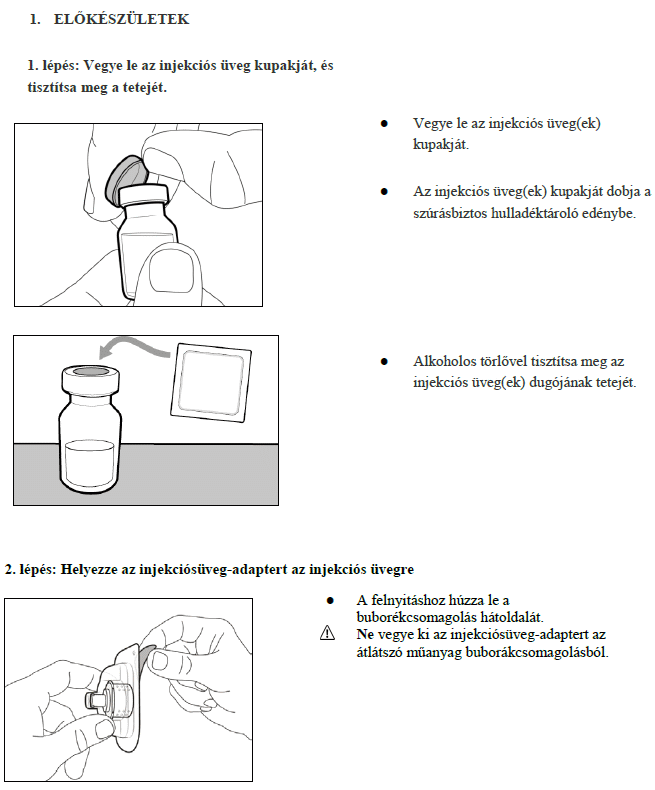
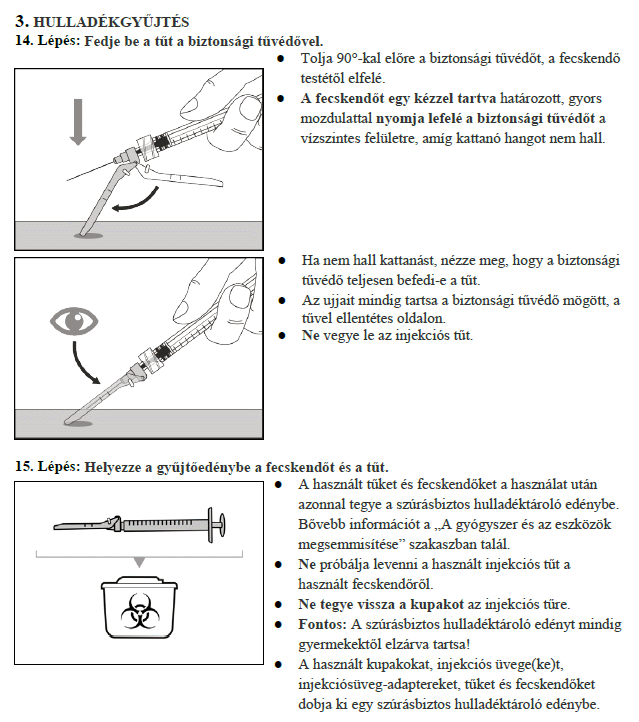
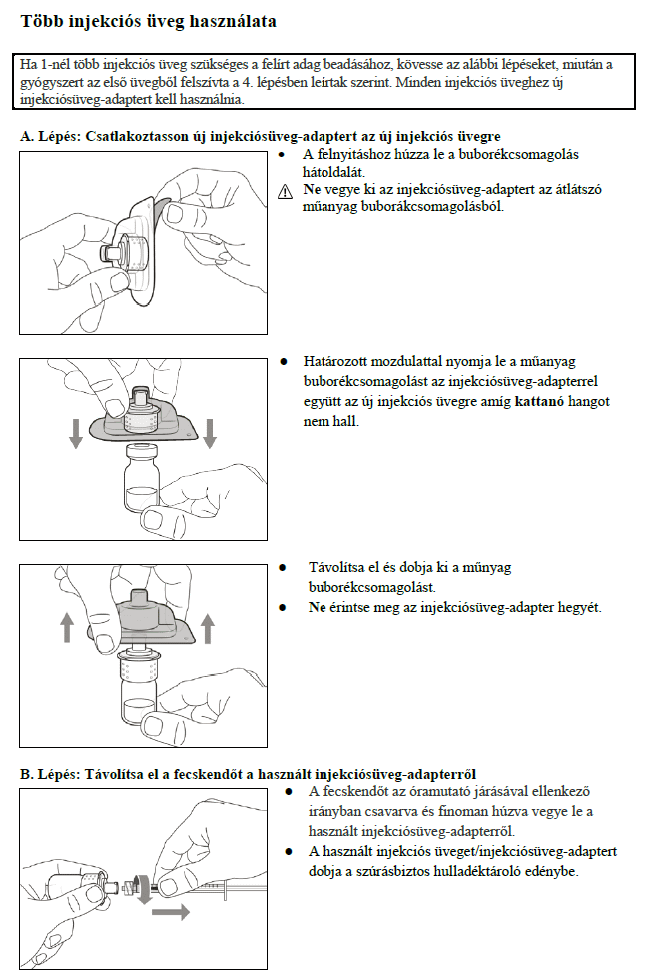
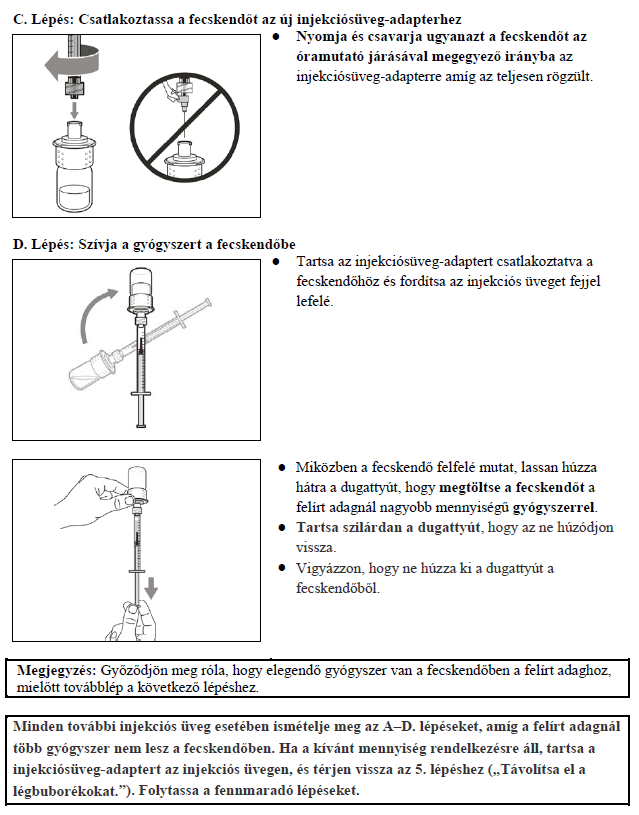
Milyen típusú gyógyszer a Hemlibra?
A Hemlibra hatóanyaga az "emicizumab". Ez a gyógyszerek "monoklonális ellenanyagok" elnevezésű csoportjába tartozik. A monoklonális ellenanyagok olyan típusú fehérjék, amelyek felismernek egy bizonyos célpontot a szervezetben és kötődnek ahhoz.
Milyen betegségek esetén alkalmazható a Hemlibra?
A Hemlibra olyan gyógyszer, amely bármely életkorban alkalmazható hemofília A-ban (veleszületett VIII-as faktor hiány) szenvedő betegek kezelésére, akiknél:
- VIII-as faktor elleni gátlóanyagok alakultak ki
- nem alakultak ki VIII-as faktor elleni gátlóanyagok és:
-- súlyos betegségben (a VIII-as faktor szintje a vérben kevesebb mint 1%) szenvednek
-- közepesen súlyos betegségben (a VIII-as faktor szintje a vérben 1% és 5% közötti) szenvednek, súlyos vérzéses fenotípussal.
A hemofília A egy veleszületett rendellenesség, melyet a véralvadáshoz és bármilyen vérzés megállításához nélkülözhetetlen VIII-as faktor hiánya okoz.
Ez a gyógyszer megelőzi a vérzéseket vagy csökkenti a vérzéses epizódok számát az említett betegséggel élőknél.
A hemofília A-ban szenvedő betegek némelyikénél VIII-as faktor elleni gátlóanyagok képződhetnek (VIII-as faktor elleni antitestek), amelyek megakadályozzák, hogy a pótlásként alkalmazott VIII-as faktor kifejtse a hatását.
Hogyan fejti ki a hatását a Hemlibra?
A Hemlibra helyreállítja a hatékony véralvadáshoz szükséges aktivált VIII-as faktor hiányzó funkcióját. A Hemlibra szerkezete eltérő a VIII-as faktor szerkezetétől, így a VIII-as faktor elleni gátló anyagok nem befolyásolják a Hemlibra hatását.
2. Tudnivalók a Hemlibra alkalmazása előtt
Ne alkalmazza a Hemlibra-t
- ha allergiás az emicizumabra vagy a gyógyszer (6. pontban felsorolt) bármely egyéb összetevőjére. Ha nem biztos ebben, a Hemlibra alkalmazása előtt kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert
Figyelmeztetések és óvintézkedések
Nagyon fontos, hogy a Hemlibra alkalmazásának megkezdése előtt beszéljen kezelőorvosával a megkerülő aktivitású hatóanyagot tartalmazó (bypassing) (a véralvadást elősegítő gyógyszerek, melyek a VIII-as faktortól eltérő módon működnek) készítmények alkalmazásáról. Ez azért fontos, mert a megkerülő aktivitású (bypassing) készítményekkel történő kezelés változására szükség lehet a Hemlibra-terápia idején. Megkerülő aktivitású (bypassing) hatóanyag például az "aktivált protrombinkomplex-koncentrátum" (aPCC) és az "aktivált rekombináns VII-es faktor" (rFVIIa).
Súlyos és akár életveszélyes mellékhatások fordulhatnak elő, amikor az aPCC-t olyan betegeknél alkalmazzák, akik egyidejűleg Hemlibra-t is kaptak.
Potenciálisan súlyos mellékhatások a Hemlibra-kezeléssel egyidejű aPCC alkalmazás esetén:
- Vörösvértest pusztulás (trombotikus mikroangiopátia)
-- Ez egy súlyos és potenciálisan életveszélyes állapot.
-- A betegeknél ebben az állapotban az erek falának belső felszíne károsodhat, és a kis erekben vérrögök keletkezhetnek. Néhány esetben ez a vese és/vagy más szervek károsodását okozhatja.
-- Legyen óvatos, ha Önnél magas ennek az állapotnak a kockázata (korábban már előfordult Önnél ez az állapot vagy valamely családtagja szenvedett ettől), vagy ha olyan gyógyszereket szed, melyek növelhetik ezen állapot kifejlődésének a kockázatát, ilyen például a ciklosporin, kinin vagy takrolimusz.
-- Fontos, hogy felismerje a trombotikus mikroangiopátia tüneteit, ha esetleg ilyen állapot kialakulna Önnél (a tünetek felsorolása a 4. pontban található, "Lehetséges mellékhatások").
Hagyja abba a Hemlibra és az aPCC alkalmazását, és azonnal forduljon orvoshoz, ha Ön vagy gondozója a trombotikus mikroangiopátia bármilyen tünetét észleli.
- Vérrögök (tromboembólia)
-- Ritka esetekben vérrög keletkezhet az erekben és elzárhatja az ereket, mely életveszélyes lehet.
-- Fontos, hogy felismerje az ilyen vérrögképződés tüneteit, ha esetleg vérrög alakulna ki Önnél (a tünetek felsorolása a 4. pontban található, "Lehetséges mellékhatások").
Hagyja abba a Hemlibra és az aPCC alkalmazását, és azonnal forduljon orvoshoz, ha Ön vagy gondozója az erekben történő vérrögképződés bármilyen tünetét észleli.
Egyéb fontos információk a Hemlibrával kapcsolatban
- Antitestképződés (immunogenitás)
-- Azt tapasztalhatja, hogy a vérzés nem kontrollálható a gyógyszer előírt adagjával. Ez azért lehet, mert ellenanyag képződik ezzel a gyógyszerrel szemben.
Azonnal keresse fel kezelőorvosát, ha Ön vagy gondozója azt észleli, hogy a vérzések fokozódnak. Előfordulhat, hogy kezelőorvosa úgy dönt, megváltoztatja a kezelést, ha ez a gyógyszer már nem hat Önnél.
1 évesnél fiatalabb gyermekek
Az egy éves kor alatti gyermekeknél a vérkeringési rendszer még mindig fejlődik. Amennyiben az Ön gyermeke egy évesnél fiatalabb, a kezelőorvosa kizárólag a készítmény alkalmazásához köthető előnyök és kockázatok gondos mérlegelése után írhat fel Hemlibra-t az Ön gyermeke számára.
Egyéb gyógyszerek és a Hemlibra
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben alkalmazott, valamint alkalmazni tervezett egyéb gyógyszereiről.
- Megkerülő aktivitású (bypassing) hatóanyagot tartalmazó készítmény alkalmazása a Hemlibra-kezelés ideje alatt
-- A Hemlibra alkalmazásának megkezdése előtt beszéljen kezelőorvosával, és gondosan kövesse az útmutatásait arra vonatkozóan, hogy megkerülő aktivitású hatóanyagot tartalmazó készítményt, mikor, milyen adagban és milyen ütemezés szerint alkalmazzon. A Hemlibra fokozza a vér alvadási készségét. Ezért a megkerülő aktivitású hatóanyagot tartalmazó készítményből kisebb adagra lehet szükség, mint amelyet a Hemlibra alkalmazása előtt kapott.
-- Csak akkor alkalmazza az aPCC-t, ha más kezelési lehetőség nem áll rendelkezésre. Ha azonban aPCC alkalmazása szükséges, beszéljen kezelőorvosával, ha úgy érzi, hogy összesen 50 egység/ttkg adagnál több aPCC beadását igényli. Az aPCC Hemlibra-kezelés ideje alatti alkalmazásáról a 2. pontban talál bővebb információt: "Potenciálisan súlyos mellékhatások a Hemlibra-kezeléssel egyidejű aPCC alkalmazás esetén".
-- Annak ellenére, hogy korlátozott tapasztalat áll rendelkezésre az anti-fibrinolitikumok aPCC-vel vagy aktivált rekombináns VII-es faktorral való együttes alkalmazásáról Hemlibra-val kezelt betegeknél, tudnia kell, hogy fennállhat a trombózisos események lehetősége anti-fibrinolitikumok intravénás alkalmazásakor aPCC-vel vagy aktivált rekombináns VII-es faktorral való kombináció esetén.
Laboratóriumi vizsgálatok
A véralvadás jellemzőit mérő laboratóriumi vizsgálatok előtt mondja el kezelőorvosának, hogy Hemlibra-t alkalmaz. Erre azért van szükség, mert a Hemlibra jelenléte a vérben befolyásolhatja a laboratóriumi vizsgálatok egy részét, ami pontatlan eredményekhez vezet.
Terhesség és szoptatás
- A Hemlibra-kezelés ideje alatt és a Hemlibra utolsó injekciójának beadását követő 6 hónapban hatékony fogamzásgátló módszert kell alkalmaznia.
- Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével. Kezelőorvosa mérlegelni fogja a Hemlibra-kezelés Önnél várható előnyeit a gyermekét érintő kockázattal szemben.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Nem valószínű, hogy ez a gyógyszer befolyásolja a gépjárművezetéshez és a gépek kezeléséhez szükséges képességeket.
3. Hogyan kell alkalmazni a Hemlibra-t?
A Hemlibra egyszer használatos injekciós üvegekben található, mint beadásra kész oldat, hígítani nem szükséges. A Hemlibra-kezelést egy vérzékeny betegek ellátásában jártas orvos fogja elindítani. A gyógyszert mindig a kezelőorvosa által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát.
Napló vezetése
A Hemlibra minden egyes alkalmazásakor írja fel a gyógyszer nevét és gyártási tételének számát.
Mennyi Hemlibra-t kell alkalmazni?
A Hemlibra adagja az Ön testtömegétől függ, és kezelőorvosa ki fogja számítani a Hemlibra beadandó szükséges mennyiségét (mg-ban) és a neki megfelelő oldat térfogatát (ml-ben).
- Telítő dózis: 1-4. hét: Az adag testtömegkilogrammonként 3 milligramm, hetente egyszer, injekcióként beadva.
- Fenntartó dózis: Az 5. héttől kezdve: Az adag vagy testtömegkilogrammonként 1,5 milligramm, hetente egyszer, injekcióként beadva, vagy testtömegkilogrammonként 3 milligramm, kéthetente, injekciónként alkalmazva vagy testtömegkilogrammonként 6 milligramm, négyhetente, injekciónként alkalmazva.
A hetente egyszer 1,5 mg/ttkg, kéthetente 3 mg/ttkg, vagy négyhetente 6 mg/ttkg fenntartó dózist alkalmazásáról való döntést a kezelőorvossal és ha releváns a gondozóval kell megbeszélni.
Az alkalmazandó teljes térfogat elkészítésénél a különböző koncentrációjú Hemlibra készítmények (30 mg/ml és 150 mg/ml) nem kombinálhatóak egyetlen injekcióban.
A beadandó Hemlibra oldat mennyisége injekciónként 2 ml-nél nagyobb nem lehet.
Hogyan kell a Hemlibra-t beadni?
Ha Ön vagy gondozója adja be a Hemlibra injekciót, gondosan el kell olvasnia és követnie kell Önnek vagy gondozójának a "Használati utasítás" című 7. pontban szereplő útmutatást.
- A Hemlibra-t bőr alá adott (szubkután) injekcióval kell alkalmazni.
- Kezelőorvosa vagy a gondozását végző egészségügyi szakember megmutatja Önnek, hogyan kell a Hemlibra injekciót beadni.
- Ha Ön oktatásban részesült, otthon, önállóan vagy a gondozó segítségével be kell tudnia adni a gyógyszert.
- Ahhoz, hogy a tűt megfelelően szúrja a bőr alá, a szabad kezével fogjon össze lazán egy bőrredőt az injekció beadásának megtisztított helyén. A bőrredő összefogása fontos annak érdekében, hogy a készítményt bőr alá (zsírszövetbe), de ne mélyebbre (izomba) fecskendezze. Az izomba adott injekció kellemetlen lehet.
- Az injekció előkészítését és beadását tiszta és csíramentes körülmények között, "aszeptikus technika" alkalmazásával végezze. Erről a kezelőorvos vagy a gondozását végző egészségügyi szakember fogja részletesebben tájékoztatni.
Hová adja a Hemlibra injekciót?
- Kezelőorvosa megmutatja Önnek, hogy a Hemlibra injekciót a test mely területeire kell beadni.
- Az injekció beadására javasolt helyek: a has alsó része, a felkar külső felszíne, valamint a comb elülső része. Kizárólag a javasolt helyekre adjon be injekciót!
- Minden alkalommal az előzőtől eltérő testtájra kell beszúrni az injekciót.
- Az injekciókat ne adja olyan helyre, ahol a bőrön bőrpír, véraláfutás, érzékenység vagy kemény terület észlelhető, illetve anyajegyek vagy hegek területére.
- A Hemlibra alkalmazásakor az egyéb, bőr alá fecskendezett gyógyszereket más területre kell beadni.
Fecskendők és tűk használata
- Egy fecskendőt, egy 5 mikrométeres szűrővel ellátott felszívó tűt vagy egy 5 mikrométeres szűrővel ellátott injekciósüveg-adaptert és egy injekciós tűt használnak ahhoz, hogy a Hemlibra oldatot az injekciós üvegből felszívják a fecskendőbe, és a bőr alá beadják.
- A fecskendők, szűrővel ellátott felszívó tűk vagy a szűrővel ellátott injekciósüveg-adapter és injekciós tűk nem találhatók meg ebben a csomagolásban. Bővebb információa 6. pontban található "Mi szükséges még a Hemlibra beadásához ami nem található ebben a csomagolásban?" cím alatt.
- Ügyeljen rá, hogy minden injekcióhoz új injekciós tűt használjon, és egyszeri használat után dobja ki.
- Legfeljebb 1 ml-es Hemlibra oldat injekcióként történő beadásához 1 ml-es fecskendőt kell használni.
- 1 ml-nél nagyobb és legfeljebb 2 ml-es Hemlibra oldat injekcióként történő beadásához 2-3 ml-es fecskendőt kell használni.
Alkalmazás gyermekeknél és serdülőknél
A Hemlibra bármilyen korú gyermekeknél és serdülőknél alkalmazható.
- Egy gyermek beadhatja saját magának a gyógyszert, a gyermek gondozását végző egészségügyi szakember és a szülő vagy gondozó beleegyezése esetén. Az öninjekciózás 7 évesnél fiatalabb gyermekek esetében nem ajánlott.
Ha az előírtnál több Hemlibra-t alkalmazott
Ha Ön az előírtnál több Hemlibra-t alkalmazott, azonnal tájékoztassa a kezelőorvosát. Ez azért szükséges, mert fennállhat a mellékhatások, például vérrögök kialakulásának kockázata. A Hemlibra-t mindig pontosan a kezelőorvosa által elmondottaknak megfelelően alkalmazza, és bizonytalanság esetén kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
Ha elfelejtette alkalmazni a Hemlibra-t
- Ha elfelejti a tervezett injekciót, adja be az elfelejtett adagot, amint lehet, a következő tervezett adag napja előtt. Ezután a tervezett módon folytassa a gyógyszer egyszer esedékes injekcióit. Ne adjon be egy napon két adagot a kihagyott adag pótlására.
- Ha nem biztos abban, hogy mit kell tennie, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
Ha abbahagyja a Hemlibra alkalmazását
Ne hagyja abba a Hemlibra alkalmazását anélkül, hogy ezt kezelőorvosával megbeszélné. Ha abbahagyja a Hemlibra alkalmazását, lehetséges, hogy már nem lesz védve a vérzésekkel szemben.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Az aPCC alkalmazásának súlyos mellékhatásai Hemlibra-kezelés ideje alatt
Hagyja abba a Hemlibra és az aPCC alkalmazását, és azonnal beszéljen egy orvossal, ha Ön vagy gondozója az alábbi mellékhatások bármelyikét észleli:
- Vörösvértest pusztulás (trombotikus mikroangiopátia):
-- zavartság, gyengeség, a karok és a lábak feldagadása, a bőr és a szemek besárgulása, nem körülírható hasi fájdalom vagy hátfájás, hányinger, hányás vagy csökkent vizeletürítés - ezek a tünetek a trombózisos mikroangiopátia jelei lehetnek.
- Vérrögök (tromboembólia):
-- duzzanat, melegség, fájdalom vagy vörösség - ezek a tünetek a bőr felszínéhez közel eső vénában keletkezett vérrög jelei lehetnek.
-- fejfájás, az arc zsibbadása, a szem fájdalma vagy duzzanata vagy látásromlás - ezek a tünetek a szem mögötti vénában keletkezett vérrög jelei lehetnek.
-- a bőr elfeketedése - ez a tünet a bőrszövet súlyos károsodásának jele lehet.
Egyéb mellékhatások a Hemlibra alkalmazása során
Nagyon gyakori: 10 beteg közül 1-nél többet érinthet
- reakció az injekció beadásának helyén (bőrpír, viszketés, fájdalom)
- fejfájás
- ízületi fájdalom
Gyakori: 10 beteg közül legfeljebb 1-et érinthet
- láz
- izomfájdalom
- hasmenés
- viszkető kiütés vagy csalánkiütés (urtikária)
- bőrkiütés
Nem gyakori: 100 beteg közül legfeljebb 1-et érinthet
- vörösvértest pusztulás (trombotikus mikroangiopátia)
- vérrög a szem mögötti vénában (szinusz kavernozusz trombózis)
- a bőrszövet súlyos károsodása (bőrelhalás)
- vérrög a bőr felszínéhez közel eső vénában (felületes tromboflebitisz)
- arc-, nyelv- és/vagy torokduzzanat és/vagy nyelési nehézség vagy csalánkiütés légzési nehézséggel társulva angioödémára utalhatnak
- a hatás hiánya vagy csökkent válasz a kezelésre
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a https://mellekhatas.ogyei.gov.hu/ weboldalon. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Hemlibra-t tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A dobozon és a címkén feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Hűtőszekrényben (2 °C - 8 °C) tárolandó. Nem fagyasztható!
A fénytől való védelem érdekében tartsa az eredeti csomagolásban.
Ha a hűtőszekrényből kivették, a bontatlan injekciós üvegek legfeljebb 7 napig tarthatók szobahőmérsékleten (30 °C alatt). Szobahőmérsékleten való tárolást követően a bontatlan injekciós üvegek a hűtőszekrénybe visszahelyezhetők. A gyógyszer szobahőmérsékleten való tárolásának összesített időtartama nem haladhatja meg a 7 napot.
Dobja ki azokat az injekciós üvegeket, amelyek több mint 7 napig voltak szobahőmérsékleten vagy amelyeket, 30 °C feletti hőmérsékleten tárolt.
Ha a Hemlibra-t az injekciós üvegből felszívták a fecskendőbe, azonnal fel kell használni. A fecskendőben levő oldatot ne tegye hűtőszekrénybe.
A gyógyszer felhasználása előtt ellenőrizze, hogy láthatók-e az oldatban részecskék vagy elszíneződés. Az oldatnak színtelennek vagy enyhén sárgásnak kell lennie. Ne használja fel a gyógyszert, ha az homályos, elszíneződött vagy látható részecskéket tartalmaz.
A fel nem használt oldatot megfelelően ki kell dobni. Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Hemlibra?
- Hatóanyaga az emicizumab. A Hemlibra injekciós üvegenként 60 mg (0,4 ml 150 mg/ml koncentrációban), 105 mg (0,7 ml 150 mg/ml-es koncentrációban), 150 mg (1 ml 150 mg/ml-es koncentrációban) vagy 300 mg (2 ml 150 mg/ml-es koncentrációban) emicizumabot tartalmaz.
- További összetevői: L-arginin, L-hisztidin, L-aszparaginsav, poloxamer 188 és injekcióhoz való víz.
Milyen a Hemlibra külleme és mit tartalmaz a csomagolás?
A Hemlibra egy oldatos injekció. A Hemlibra színtelen/enyhén sárgás folyadék.
A Hemlibra minden csomagja 1 injekciós üveget tartalmaz.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Mi szükséges még a Hemlibra beadásához, ami nem található ebben a csomagban?
Egy fecskendőre, egy szűrővel ellátott felszívótűre vagy szűrővel ellátott injekciósüveg-adapterre és egy injekciós tűre van szükség ahhoz, hogy a Hemlibra oldatot az injekciós üvegből egy fecskendőbe felszívják és a bőr alá fecskendezzék (lásd 7. pont, "Használati utasítás").
Fecskendők
- 1 ml-es fecskendő: Átlátszó polipropilén vagy polikarbonát fecskendő Luer-záras tűvel, 0,01 ml-enkénti osztással, vagy
- 2-3 ml-es fecskendő: Átlátszó polipropilén vagy polikarbonát fecskendő Luer-záras tűvel, 0,1 ml-enkénti osztással.
Megjegyzés: Kis holtterű (LDS) dugattyúval ellátott fecskendőket kell használni a szűrővel ellátott injekciósüveg-adapter használatakor.
Felszívó eszközök és tűk
- Szűrővel ellátott felszívó tű: Rozsdamentes acél, Luer-záras csatlakozós, külső átmérője 18 G, hossza 35 mm (11/2″), 5 mikrométeres szűrővel ellátott, lehetőleg félig tompa heggyel, vagy
- Szűrővel ellátott injekciósüveg-adapter: polipropilén, Luer-záras csatlakozós, 5 mikrométeres szűrővel, 15 mm-es injekciós üveg nyakátmérővel és
- Injekciós tű: Rozsdamentes acél, Luer-záras csatlakozós, külső átmérője 26 G (elfogadható tartomány: 25 - 27 G), hossza lehetőleg 9 mm (3/8″) vagy legfeljebb 13 mm (1/2″), lehetőleg a biztonsági tűvédő elemet is beleértve.
7. Használati utasítás































Fogyasztói ár:
1607748Ft
A feltüntetett ár tájékoztató jellegű, patikánként kisebb-nagyobb eltérés előfordulhat.
Normatív támogatás esetén téritési díj: 1607748 Ft
Fogyasztói ár:
2812781Ft
A feltüntetett ár tájékoztató jellegű, patikánként kisebb-nagyobb eltérés előfordulhat.
Normatív támogatás esetén téritési díj: 2812781 Ft
Fogyasztói ár:
4017812Ft
A feltüntetett ár tájékoztató jellegű, patikánként kisebb-nagyobb eltérés előfordulhat.
Normatív támogatás esetén téritési díj: 4017812 Ft
 Az adatokat a PHARMINDEX gyógyszer-információs adatbázis szolgáltatja. © Vidal Next Kft. 2024
Az adatokat a PHARMINDEX gyógyszer-információs adatbázis szolgáltatja. © Vidal Next Kft. 2024

























